2022年09月
HIF-PH阻害薬使用時の血栓塞栓症リスクを考える
院長の山嵜です。
本日は「HIF-PH阻害剤のBest Use ~専門医とひも解く腎性貧血治療~」の会で「HIF-PH阻害薬使用時の血栓塞栓症リスクを考える」というテーマでお話をさせて頂きました。
HIF-PH阻害薬を使用する上で注意すべきポイントの一つが血栓塞栓症の存在です。
2020年に腎臓学会から発表されました「HIF-PH阻害薬適正使用に関するrecommendation」でも血栓塞栓症に対する注意喚起が行われています。
HIF-PH阻害薬使用時に注目すべき3つの血栓症リスク
① Hbの過剰な増加、急速なHb増加
② 鉄欠乏の存在
③ 悪性腫瘍の存在
Hbの目標値は
① 保存期慢性腎臓病:11-13g/dL
② 透析期慢性腎臓病:10-12g/dL
とされており、過剰なHbの増加は赤血球凝集亢進を介して凝固系を促進させること、またブラッドアクセスの血栓症も多いことが知られています。
また、HIF-PH阻害薬使用時の急激なHb上昇も血栓塞栓症発症のリスクと考えられており、Hbの上昇速度が0.5g/dL/weekを超えないようにすることが推奨されています。

もう一つ血栓塞栓症のリスクとなる得るのが鉄欠乏の存在です。
鉄欠乏性貧血では巨核球の分化が進み、血小板増多をきたすことが知られています。
そして、血小板増多を認める鉄欠乏性貧血患者では血栓症の罹患率が高いことが報告されています。

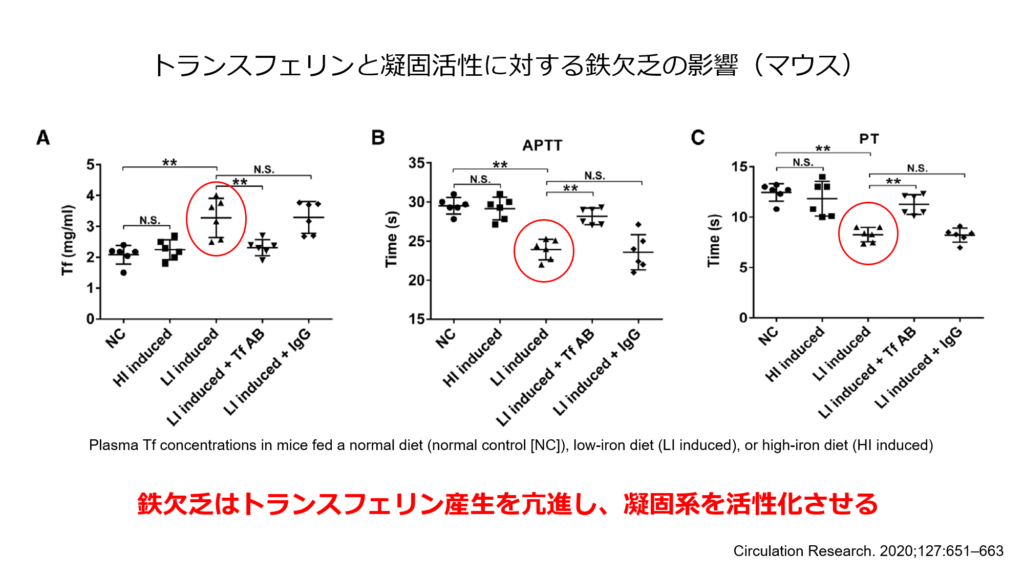
鉄欠乏ではトランスフェリンの産生が増加し、このトランスフェリンの増加も血栓症のリスクであることが報告されています。
鉄の少ない食事を与えた鉄欠乏マウスではトランスフェリンが増加し、それに伴いPT・APTTが短縮する事が明らかとなりました。
また、鉄欠乏のマウスの頸動脈血流は低下しており、そのマウスに抗トランスフェリン抗体を投与すると頸動脈血流が改善することから、鉄欠乏に伴うトランスフェリンの増加が血液の粘稠度を上げることで血流が低下していることが示唆される結果と考えられます。
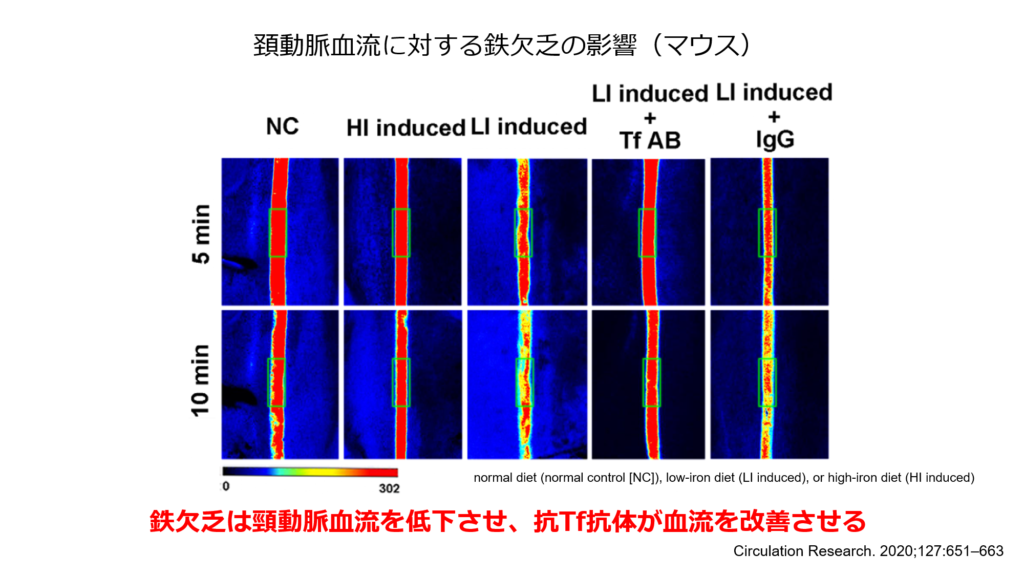
以上のように鉄欠乏は血栓症リスクを上昇させることから、HIF-PH阻害薬使用前には必ず鉄動態を評価する事が重要です。
鉄欠乏の評価はフェリチンとTSAT(トランスフェリン飽和度)で行います。
【鉄欠乏の指標】
・フェリチン<100μg/L
・TSAT(%):(血清鉄/TIBC)×100<20%
上記による評価にてHIF-PH阻害薬使用前に鉄欠乏が存在しているようであれば、まずは鉄の補充を行い貧血の改善度を確認します。
またHIF-PH阻害薬使用後に鉄利用能が改善し鉄欠乏が生じることがありますので、HIF-PH阻害薬使用後は定期的に鉄動態を評価する事も重要です。
以上HIF-PH阻害薬使用時の血栓塞栓症リスクについて述べさせて頂きました。
これまで注射剤しか存在しなかった腎性貧血の治療薬として新たに登場したHIF-PH阻害薬。
血栓塞栓症などのリスクに注意して使用すれば、その有効性は注射薬と同等であり、また内服薬であること、そして注射薬に抵抗性を有する患者様でも有効である可能性を持っていることから、腎性貧血治療において今後主役となることが期待される薬剤と言えるかもしれません。
たちばな台クリニック 山嵜 継敬
心不全患者における高カリウム血症管理
院長の山嵜です。
本日は「Cardiorenal Conference ~心腎について考える~」の会に参加してまいりました。

近年心不全治療は新薬が次々と登場し、目覚ましい発展を遂げています。
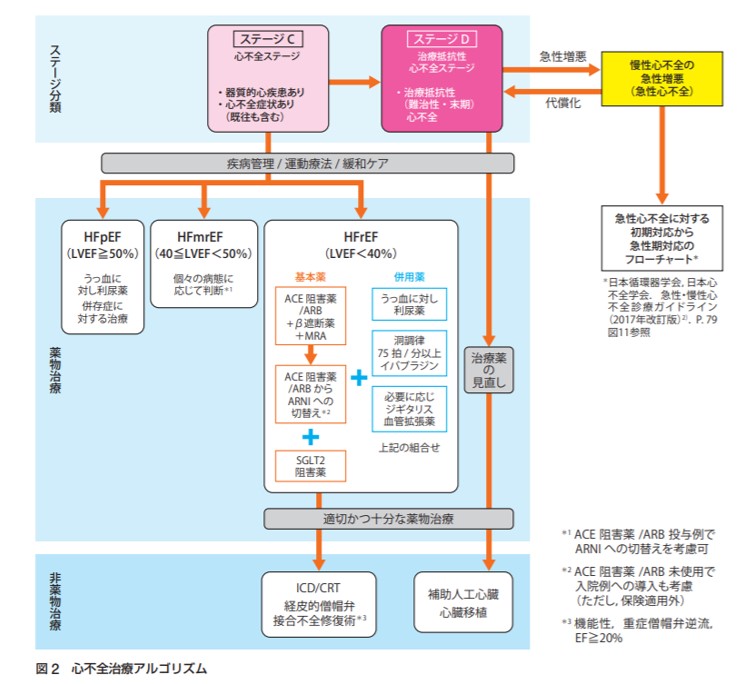
下は急性・慢性心不全診療ガイドラインフォーカスアップデート版に記載されている心不全治療アルゴリズムです。
EF<40%と左室収縮能の低下したHFrEF患者における基本薬は
・ACE阻害薬/ARB
・β遮断薬
・MRA
の3剤となっております。
海外のガイドラインではACE阻害薬/ARBよりもARNIを推奨しているものもあり、またそれにSGLT2阻害薬を加えた4剤を「Fantastic Four」と称しなるべく早期にこの4剤を投与することが予後を改善させるという報告もあります。
このような治療戦略により心不全の予後改善が期待されるわけですが、ACE阻害薬、ARB、MRAのいずれも血清カリウム値を上昇させる可能性があることから、心不全治療における高カリウム血症が問題視されるようになってきました。
心不全における高カリウム血症の要因は大きく3つ。

高カリウム血症患者は予後不良であることが知られていますが、特に高カリウム合併心不全では死亡率が上昇する事が報告されています(Am J Nephrol. 2017; 46: 213-221)。
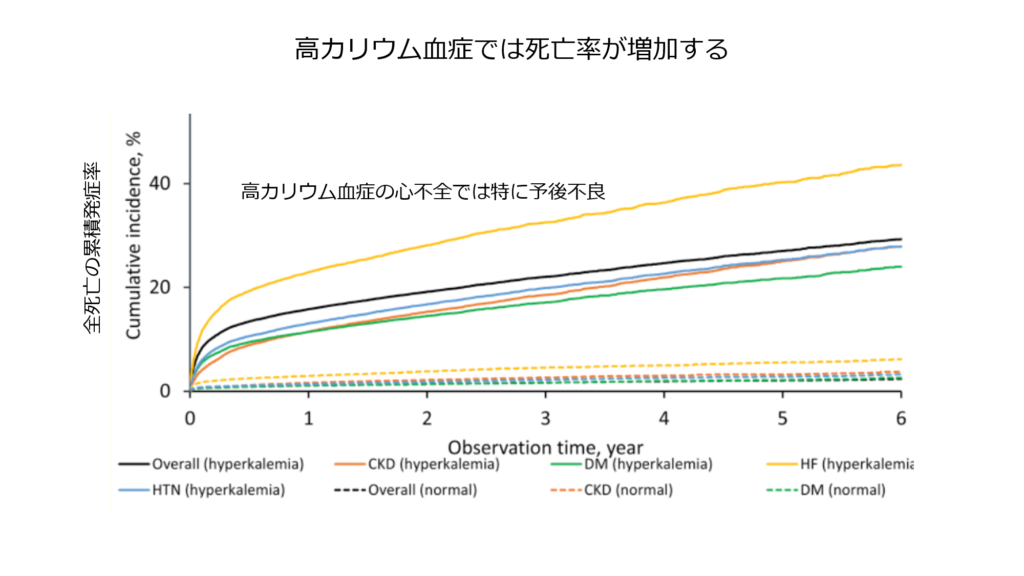
高カリウム血症でなぜ心不全の予後が不良になるのか?
その原因は高カリウム血症自体ではなく、高カリウム血症が存在する事でRAAS阻害薬やMRAを中止してしまうことにあるという事が報告されています。
そこでRAAS阻害薬やMRAを使用する心不全患者の高カリウム闕所に対しては薬剤を減量・中止するのではなく、カリウムバインダーを使用し血清カリウム値をコントロールした上で薬剤を継続する事が推奨されるようになりました(JACC 2020; 75(22): 2836-50)。

これまでのカリウムバインダーはざらつきがあり非常に飲みにくく、ポリマー製剤であるため便秘などの副作用が多いことが問題となっていました。
近年使用可能となりましたロケルマ(ジルコニウムシクロケイ酸ナトリウム水和物)はカリウムとの選択性が高く、内服数時間からカリウム低下作用を示し、また非ポリマー性であるため便秘の副作用が比較的少ないことが特徴の薬剤です。
また水に溶かして飲むタイプのため飲みやすいことも内服の継続にはとても重要であると思われます。

高カリウム血症に対する新規薬剤の登場は、今後の心不全治療におけるRAAS阻害薬使用継続のキードラッグとなるかもしれません。
(山嵜 継敬)






