院長より
Yokohama Brain Conference
院長の山嵜です。
最強寒波の極寒の中皆様いかがお過ごしでしょうか。
本日は12月15日脳神経外科の先生を対象に開催されましたYokohama Brain Conferenceについてお話をさせて頂きたいと思います。
こちらの会では大変お世話になっております横濱もえぎ野クリニックの泉山先生にお声掛けを頂き
「高血圧診療Update ~ARNIがもたらす新たな高血圧治療戦略~」
というテーマで講演をさせて頂きました。

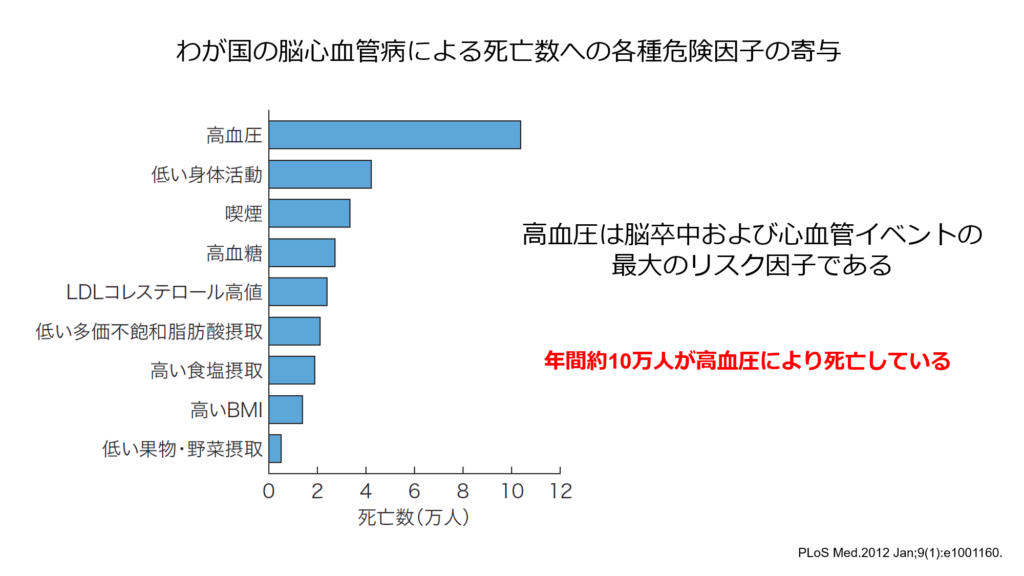
「高血圧は脳卒中および心血管イベントの最大のリスク因子である。」
これがkey wordになります。
下の図は日本においてどのようなリスク因子が脳心血管死に関与しているのかを表したグラフになりますが、圧倒的に高血圧の関与が強く、高血圧関連脳心血管死は年間約10万人におよぶと考えられております。
ではどの程度に血圧をコントロールすれば脳卒中イベントは減少するのか?
高齢であれば血圧は高くても良いのではと考えられていた時代もございましたが、現在は75歳未満の方や高度狭窄を有さない脳血管疾患の方、冠動脈疾患の既往のある方、糖尿病の方、蛋白尿を有する慢性腎臓病の方では診察室血圧を120台にコントロールする事が高血圧ガイドライン2019でも推奨されております。
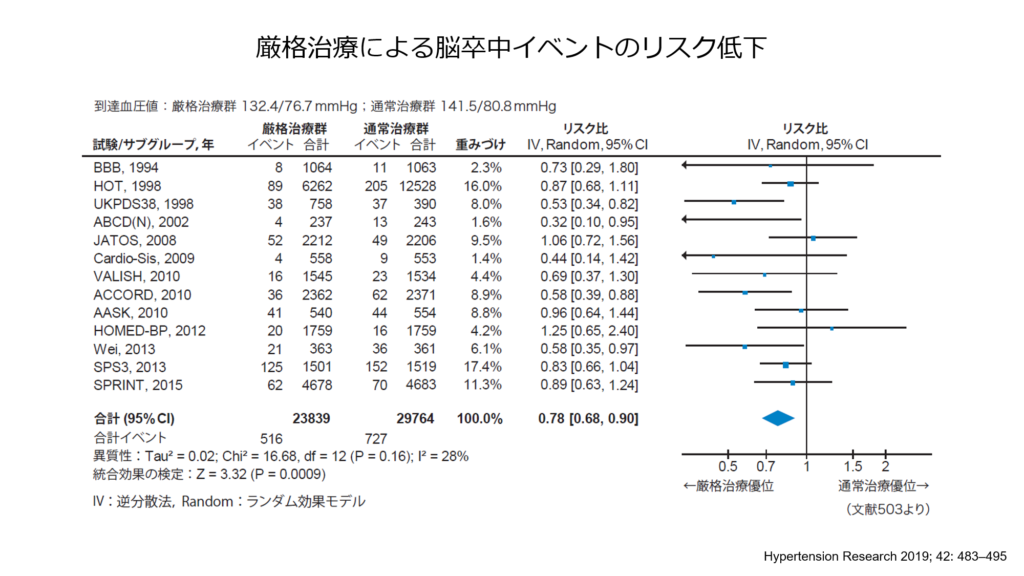
下は血圧を130を目標に治療をした方と、140を目標に治療を行った方の脳卒中イベントを評価したメタ解析になりますが、130を目標に厳格に高血圧の治療を行った群で22%脳卒中の発症リスクが低下する事が示されております。
血圧には日内変動があり、早朝高血圧が心血管イベントのリスク因子であることが知られています。
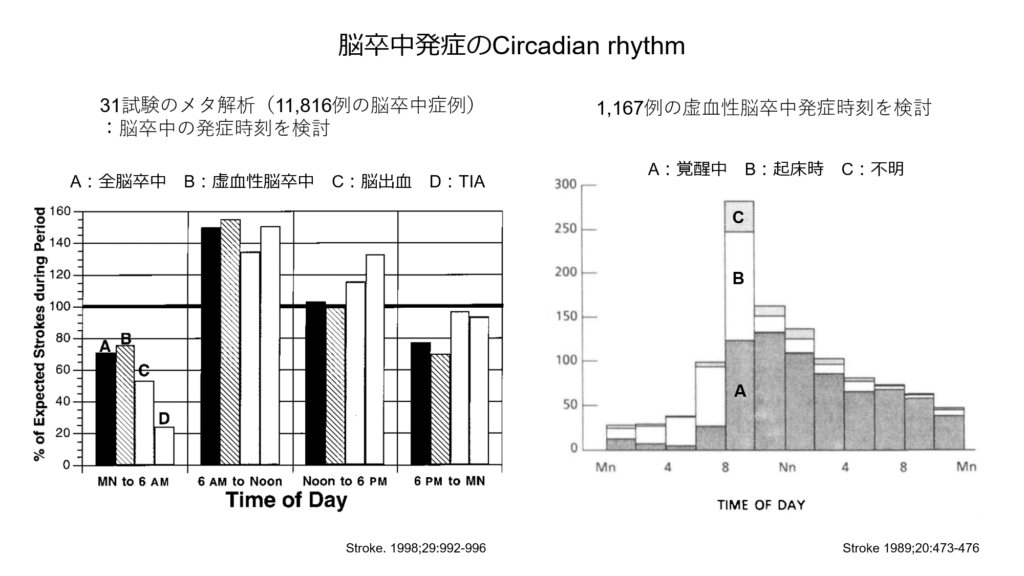
脳卒中発症にも日内変動があり、下記の2つの試験結果からも脳卒中の発症は朝から午前中にかけて多いことが報告されております。
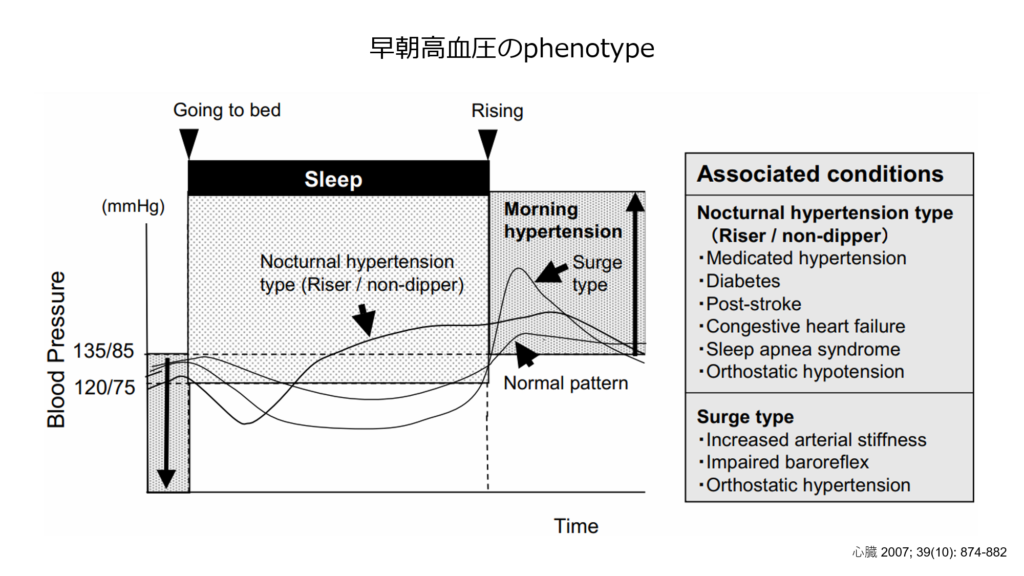
早朝高血圧は2つのタイプに分類されます。
① Surge type:朝方急激に血圧が上昇するタイプ
② Nocturnal hypertension type:夜間の血圧が高く、そのまま朝まで高いタイプ
高血圧の治療目標の一つは朝の血圧をいかにコントロールするかがポイントです。
・塩分摂取が多くないか?
・睡眠時無呼吸症候群が存在しないか?
・糖尿病、慢性腎臓病、心不全などが存在しないか?
・アルコール摂取が過剰でないか?
・不眠症がないか?
・起床後すぐに喫煙をしていないか?
・寒い部屋で眠っていないか?
などなど要因を挙げ始めればきりがありません。
高血圧の治療は降圧薬をパッと処方するだけではなく、このような要因の存在や背景にある生活習慣を考え、きめ細やかに投薬調整を行うことが重要となります。
血圧治療で何か不安なことがございましたらいつでもお気軽にご相談ください。お待ちしております。
心腎貧血症候群WEBセミナー ~今見直される鉄欠乏の重要性~
今回は前回でも予告いたしましたように、鉄欠乏の重要性についてお話をしたいと思います。
11月1日に心腎貧血症候群WEBセミナーで鉄欠乏の重要性について講演をさせて頂きました。
生体内に存在する金属元素のうち最も多く存在するのが鉄です。
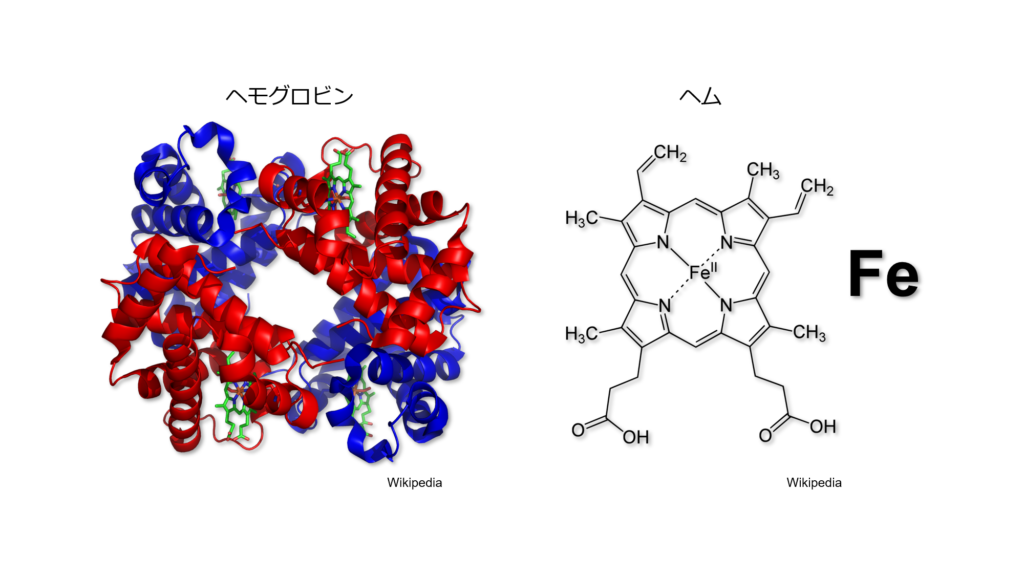
鉄は体内に約3g存在すると言われていますが、その6割は血液中のヘモグロビンの構成成分となり酸素運搬という重要な役割を果たしています。
鉄欠乏には2種類存在します。
① 絶対的鉄欠乏
② 機能的鉄欠乏
鉄欠乏を評価する上で重要な項目も2つ。
1)トランスフェリン飽和度(TSAT):血清鉄/総鉄結合能(TIBC)×100(%)
:血液を産生するために働くことのできる鉄の実働部隊と考えられます。
お金で例えるとすぐに使えるようにお財布に入っているお金と考えると良いでしょう。
2)血清フェリチン値
:肝臓などの網内系に蓄積している鉄の貯蔵量を反映しています。
お金で例えると銀行に貯金しているお金と考えると良いでしょう。
それでは2種類の鉄欠乏について
① 絶対的鉄欠乏
消化管出血などによる喪失や鉄摂取不足、吸収不良により体内の鉄絶対量が不足している状態を絶対的鉄欠乏と呼びます。
TSATは20%未満、血清フェリチン値は12-15μg/L未満、 炎症を伴っている患者で50μg/L未満(もしくはそれ以上)で鉄欠乏の診断基準と設定しています。
しかし慢性腎臓病や心不全は慢性炎症状態と考えられるため
血清フェリチン値<100μg/L, 血清フェリチン値100~300μg/Lの時はTSAT<20%で鉄欠乏と判断し鉄補充療法を検討することが推奨されています。
② 機能性鉄欠乏
急性・慢性炎症、感染症、悪性腫瘍などの病態では炎症性サイトカイン産生を介して肝臓でのヘプシジン合成が促進されます。ヘプシジンは腸管における鉄吸収や網内系細胞からの鉄放出を抑制する作用を有するため、上記の病態では鉄は網内系細胞内にとどまり鉄利用能が低下します。
そのため血清フェリチン値は増加し、実働部隊であるTSATは低値を示すことになります。
このような病態では体内における鉄の絶対量は充足しているため鉄補充は推奨されません。
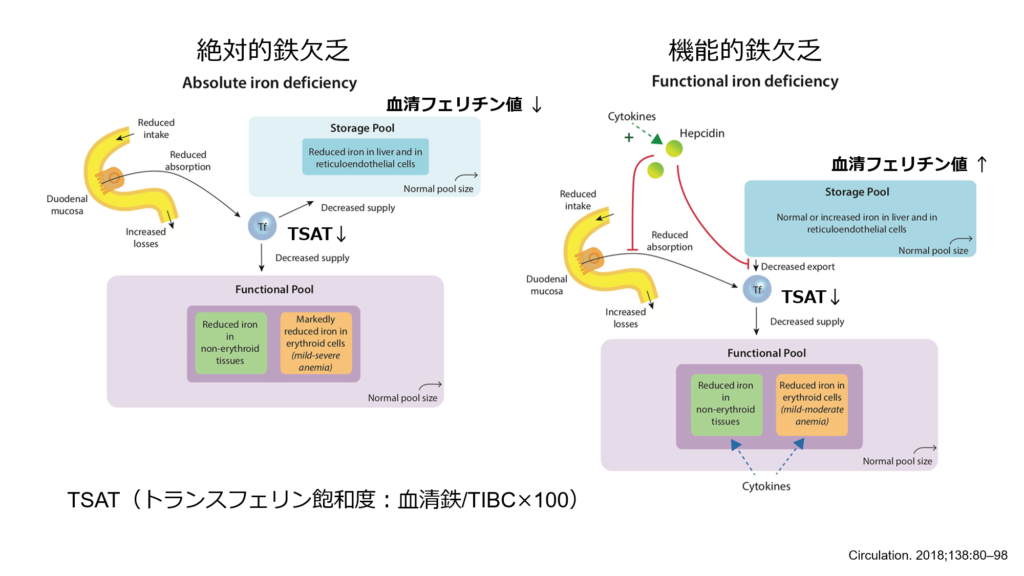
以上のように鉄欠乏の評価、鑑別にはTSATと血清フェリチン値の両指標を必ず評価する必要があります。
慢性腎臓病、心不全には鉄欠乏の合併が多いことが知られています。
また鉄欠乏と言えば鉄欠乏性貧血が有名ですが、貧血を呈していなくとも鉄欠乏が存在するだけで運動耐容能の低下や心不全の再入院率の増加をきたすことが知られています。
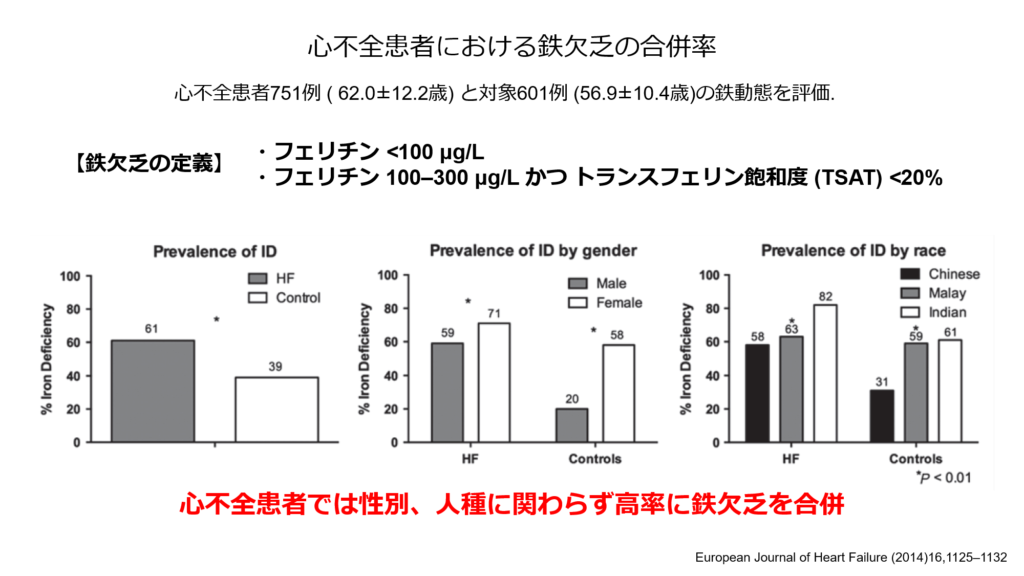
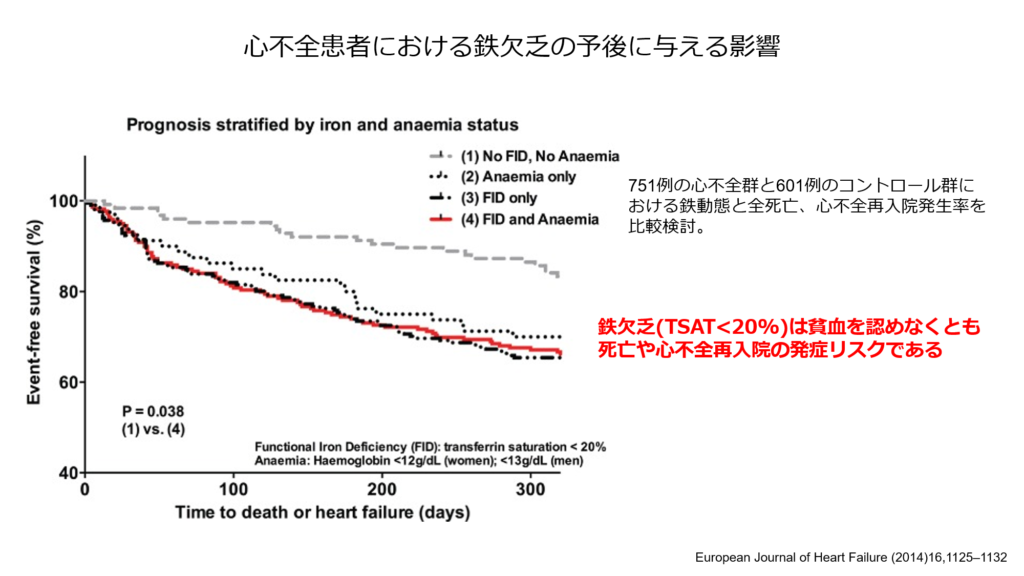
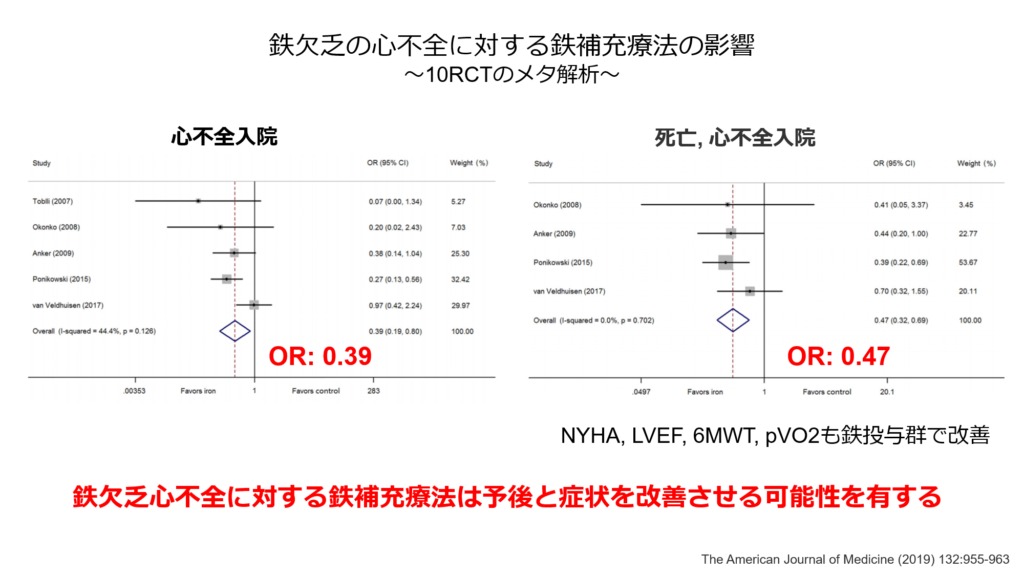
以上のように心不全に高率に合併する鉄欠乏を見逃すことなく診断、必要があれば鉄補充療法を検討する事が必要であり、鉄欠乏の心不全に対する鉄補充療法の有効性も下記に示すように報告されています。
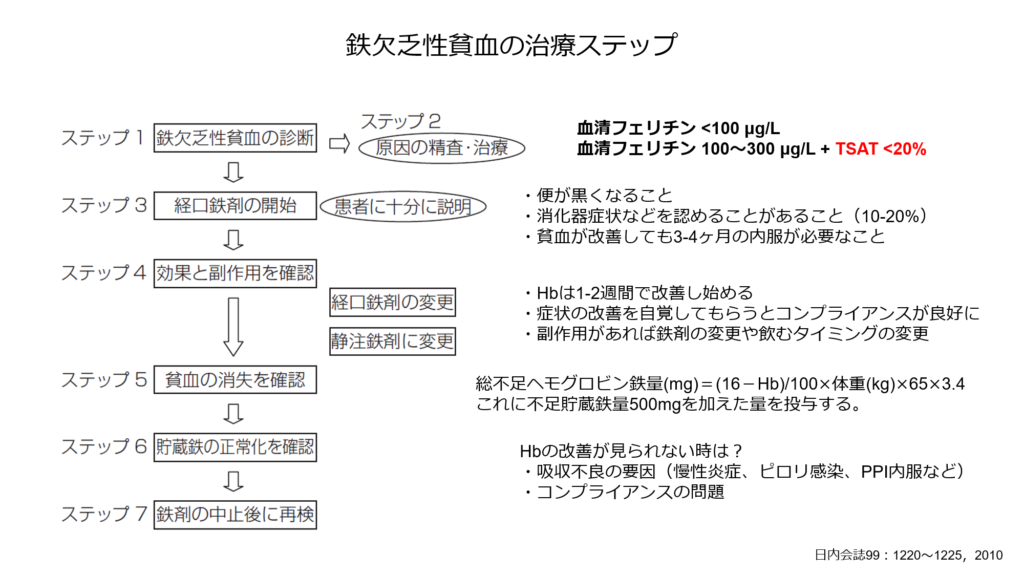
鉄欠乏性貧血の治療はまず原因の精査とTSAT、血清フェリチン値の評価。
その後はまずは経口鉄剤から治療を開始。
経口鉄剤を開始すると便が黒くなります。また副作用として胃腸症状をきたすことがあることをしっかりと説明しておくことが重要です。
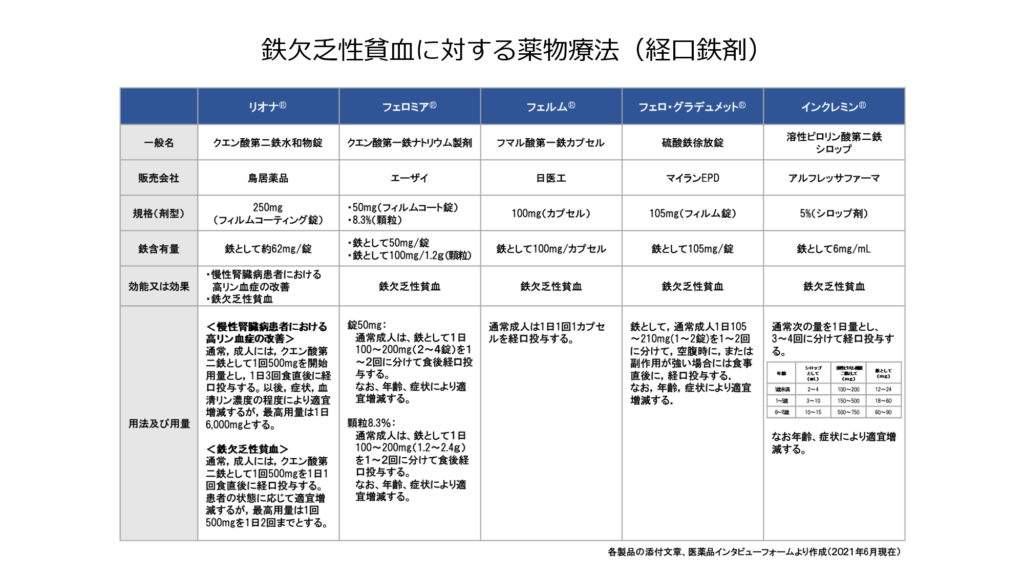
鉄剤には二価鉄を用いた製剤と三価鉄を用いた製剤があります。
吸収は二価鉄の方が良好と言われていますが、消化器症状は三価鉄の方が少ないため、鉄剤開始後吐き気などを認める時は三価鉄製剤の使用を検討するといいかもしれません。
(第一鉄→二価鉄、第二鉄→三価鉄)
以上鉄に関してお話をさせて頂きました。
体内に3gしか存在しない鉄がこれだけ重要な働きをしていることに正直驚かされます。
普段からバランスのとれた食事をすることも重要ですが、健診で貧血を指摘された方や、慢性腎臓病、心不全、その他疾患をお持ちの方で不安をお持ちの方は是非お気軽にご相談ください。
ケアネットWEB講演会 ~かかりつけ医による腎性貧血治療~
本日は2022年11月29日にケアネットWEB講演会でお話をさせて頂きました内容についてご報告をしたいと思います。
今回のテーマ
「かかりつけ医による腎性貧血治療 ~心腎貧血症候群から読み解く貧血治療の重要性~」
心疾患と慢性腎臓病の間には深い関係が存在します。
心不全では心拍出量の低下や腎潅流量の低下、レニンアンジオテンシンアルドステロン系亢進や交感神経活動の亢進、慢性炎症や吸収不良に伴う貧血などを介して慢性腎臓病を増悪させます。
一方慢性腎臓病ではナトリウム貯留や水貯留によるうっ血や高血圧、エリスロポエチン低下に伴う貧血を介して心不全を増悪させます。
このような心疾患と慢性腎臓病の関係を「心腎連関」と呼んでいますが、心不全と慢性腎臓病両疾患に深く関与する病態が貧血です。
貧血が存在する事で心不全と慢性腎臓病の悪循環が成立してしまう事から、この3つが同時に存在する病態は「心腎貧血症候群 CRAS」と呼ばれています。
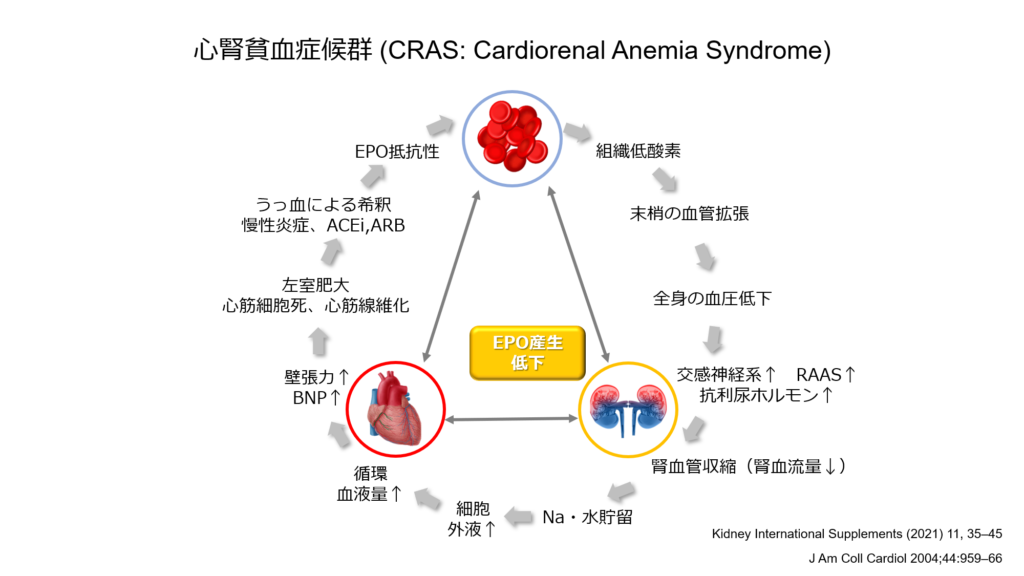
CRASが存在すると予後が不良なことは多く報告されており、慢性腎臓病や貧血を有さない心不全患者に比べ、CRASでは全死亡の発生が有意に高いことが知られています(ハザード比:2.0)。
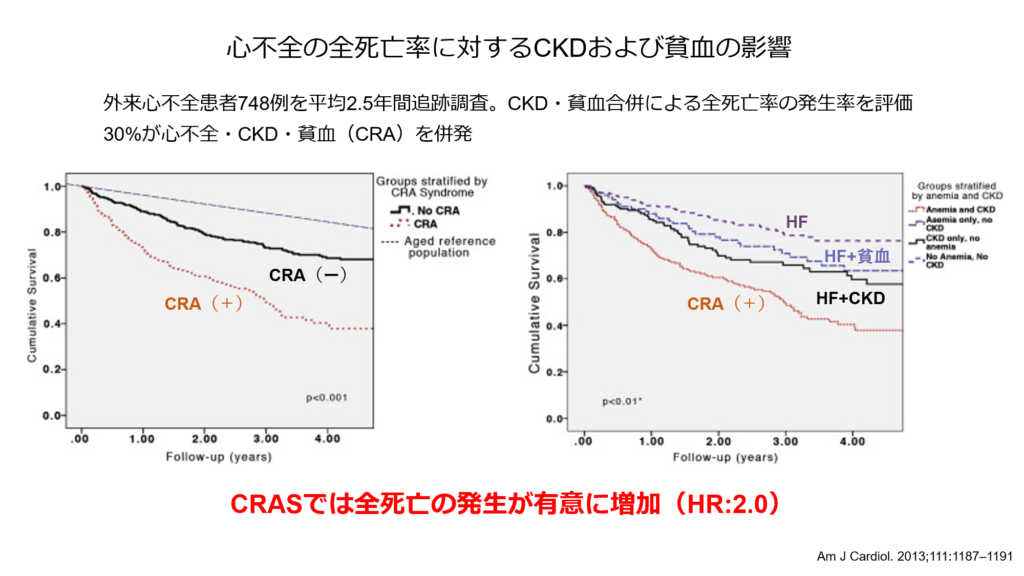
心不全・慢性腎臓病・貧血の中で比較的治療介入を行いやすいことから、近年貧血治療が注目されるようになりました。
消化管出血を含む原因疾患の鑑別が最も重要になりますが、治療介入において重要な二つの病態が
① 鉄欠乏
② 腎性貧血
です。
鉄欠乏に関しましては別の講演会でも詳しくお話をさせて頂きましたので、後日改めてブログに書かせて頂こうと思いますが、一文にまとめさせて頂きますと・・・
「鉄欠乏は心不全や慢性腎臓病に高率に合併し、息切れや心不全の予後に大きく影響するため、トランスフェリン飽和度 20%未満では鉄補充療法を検討するべきである」
という事になるかと思います。
そして次のステップと致しまして、慢性腎臓病患者で鉄補充を行っても貧血が残存し、エリスロポエチン濃度が50mlU/mLで網状赤血球の増加が見られない場合には腎性貧血を疑う必要があります。
ではヘモグロビンがどのレベルになったら治療介入を検討するべきか。
現ガイドラインでは下記のように推奨されています。
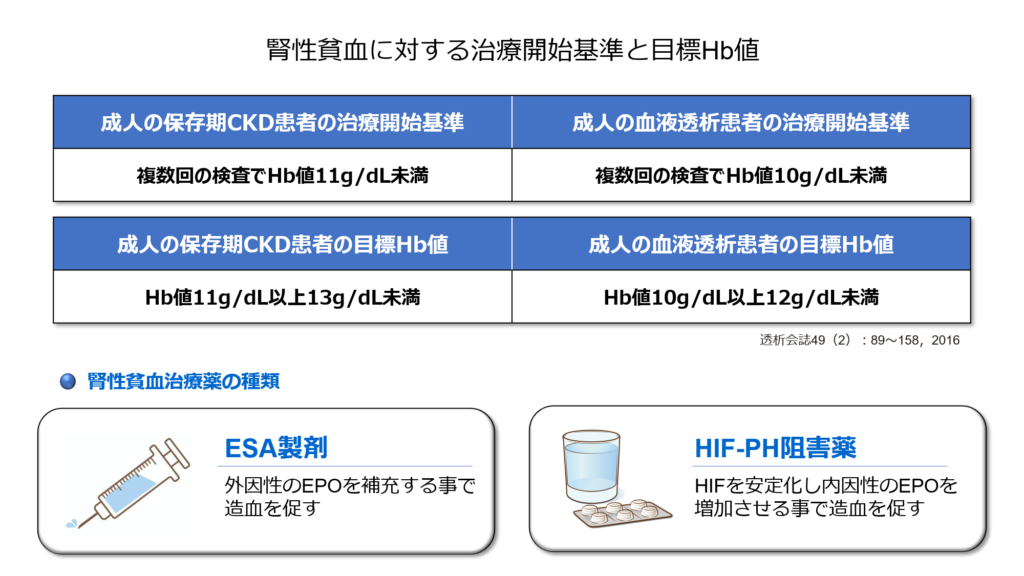
そして腎性貧血治療には「ESA製剤」と「HIF-PH阻害薬」があり、患者様の病態、生活習慣、嗜好などにより選択する事になります。
これまでも使用しており注射に慣れている、内服薬をこれ以上増やしたくない方であればESA製剤を、
注射には抵抗がある、通院する機会をなるべく減らしたい方であればHIF-PH阻害薬を
選択するメリットがあるかと思います。
またESA製剤を使用しているがなかなか貧血の改善が見られず、ESA製剤の用量が非常に多くなってしまっているような「ESA抵抗性」を示す方ではHIF-PH阻害薬に変更してみるのも手かもしれません。
ESA製剤の用量が多い方では心血管リスクが高いという報告もあり注意が必要です。
ESA抵抗性の最大の要因は鉄欠乏です。ESAを投与しても血液の素材が不足していれば貧血は改善しません。
そしてもう一つkeyとなるのが「ヘプシジン」という鉄調節因子の存在です。
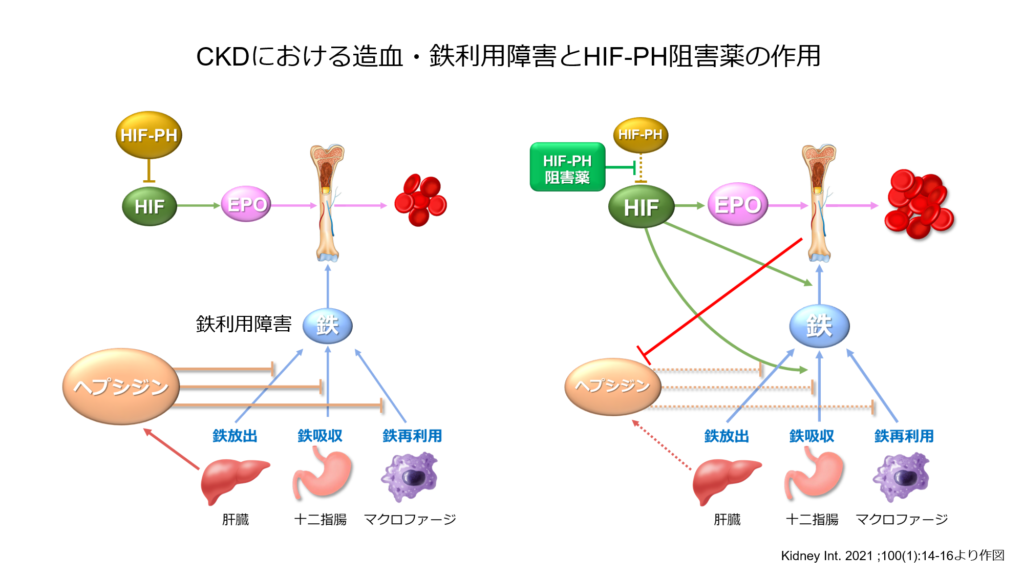
ヘプシジンは体内に鉄が過剰になった時に肝臓で生成され、腸管や網内系細胞の鉄輸送蛋白であるフェロポルチンに結合することで、消化管からの鉄吸収や網内系細胞からの鉄放出を抑制する働きを有しています。
慢性腎臓病は慢性炎症の病態を有しておりますが、増加した炎症性サイトカインはヘプシジンを増加させ、また腎機能障害下ではヘプシジンの排泄も低下するためヘプシジン濃度が上昇します。ヘプシジンが増加した状態では鉄利用能が低下してしまうためESA抵抗性が惹起されるということになるわけです。
HIF-PH阻害薬がヘプシジン濃度を低下させ、鉄利用を改善させるという臨床データがいくつか示されており、日本腎臓学会からも「ESA抵抗性の原因が不明若しくは対応が困難な場合(鉄利用障害など)には、HIF-PH阻害薬への変更を考慮しても良い」というrecommendationが発表されています。
貧血による息切れや心不全・慢性腎臓病増悪をかかりつけ医が見逃さないことが患者様にとって大きなメリットになることは間違いありません。
内服薬による腎性貧血治療という選択肢を手に入れたことにより、新たな貧血治療の時代が訪れたと言っても過言ではないでしょう。
アブレーション関連秋季大会2022
院長の山嵜です。
今日は昨年11月に新潟県朱鷺メッセで開催されました「アブレーション関連秋季大会2022」のご報告をさせて頂きたいと思います。
コロナ禍でWEB開催が続いておりましたが、今回から現地開催となりました。
本当に久しぶりの県外遠征です。新幹線には何年ぶりに乗ったでしょうか。


今回は当院で行っている心房細動アブレーション術式に関する発表をしてきました。
心房細動治療で最も重要な手技が肺静脈隔離術です。
肺静脈隔離術にも様々な手技がありますが、上下の肺静脈を1周するように大きく隔離する拡大肺静脈隔離術が現在主流となっております。
拡大肺静脈隔離術の弱点は1ポイントでも再伝導をしてしまうと心房細動の再発リスクが高くなるという点です。
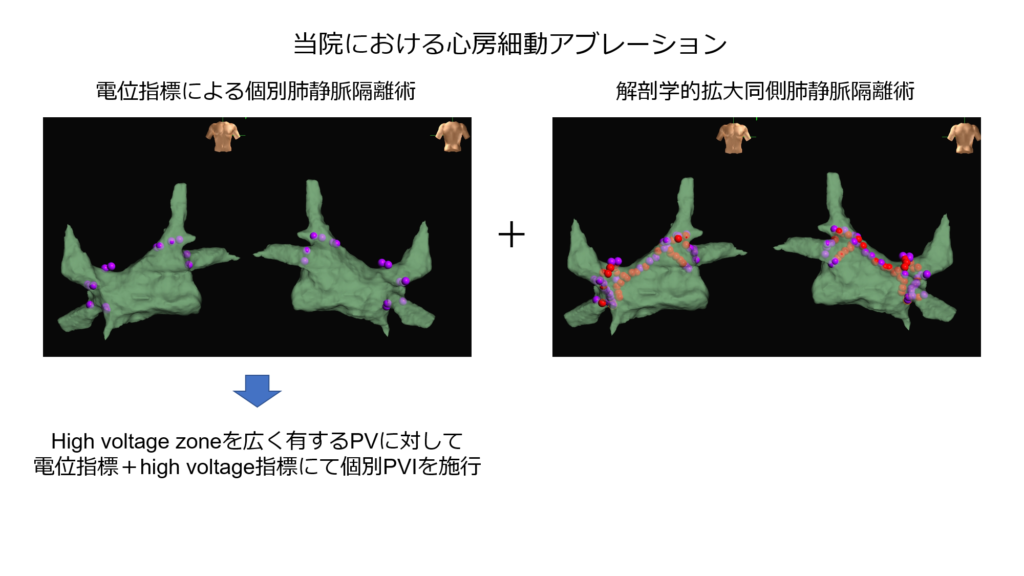
一方左心房と肺静脈間の電気的交通部位を電位からpoint-by-pointで標的を定めて治療する個別肺静脈隔離術は少ない通電ポイントで治療を行うことが出来る点がメリットになります。
しかし、肺静脈外・前庭部起源の異常興奮には効果がないことが弱点となります。
そこで私たちははじめに少ないポイントで個別肺静脈隔離術を施行し、その後大きく拡大肺静脈隔離術を行うハイブリッドアブレーションを行い、再発が少しでも少なくなるように治療を行っております。
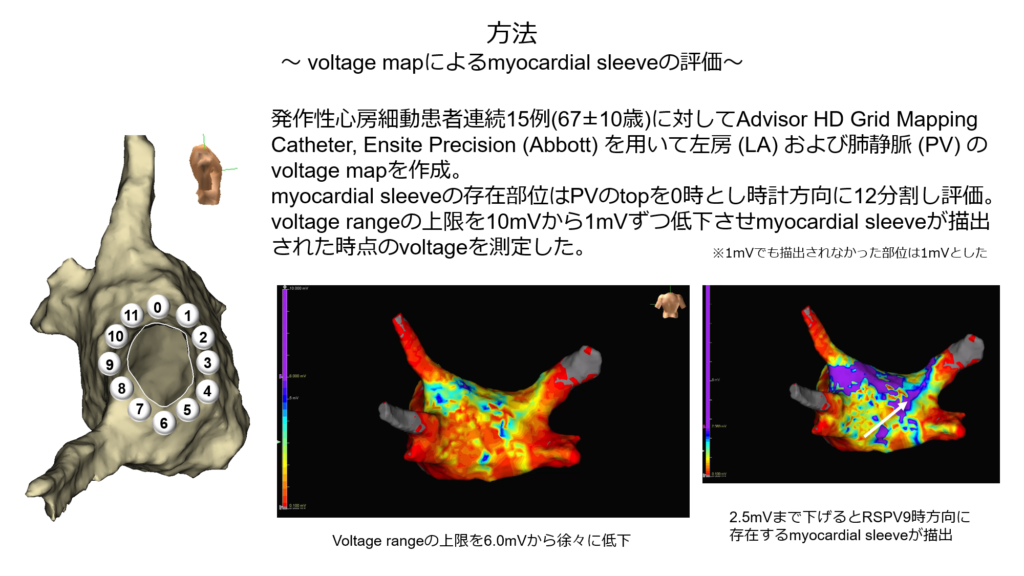
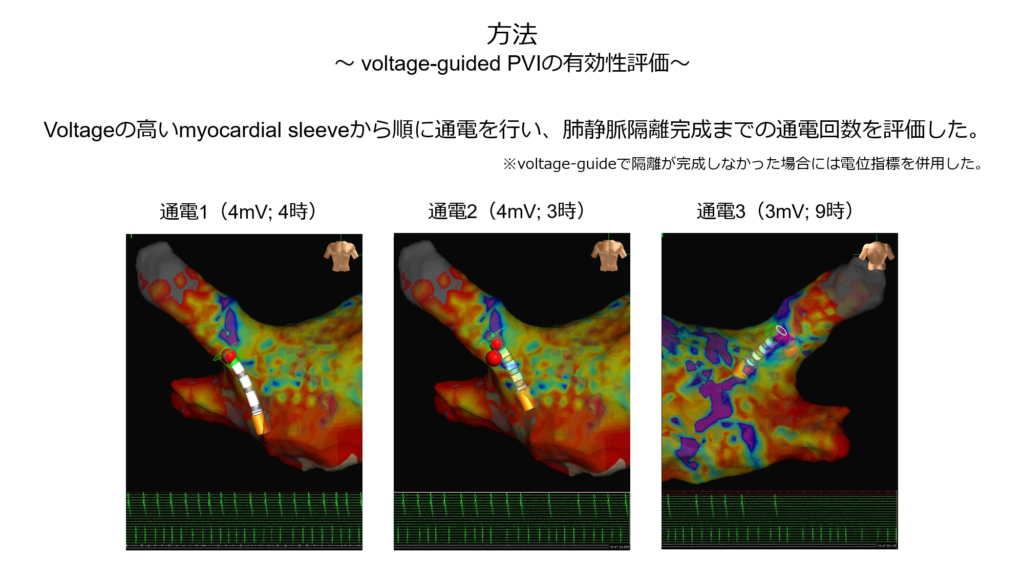
その際に電位指標だけでは個別隔離が困難な症例も存在するため、voltage mapを作成し電位の高い部位を標的に通電を行うvoltage指標アブレーションも併用しています。
今回の発表では
① 各肺静脈の電位にはどのような特徴があるか?
② voltage map指標で個別隔離術を行った際に何回の通電で隔離を成功することが出来るか?
について研究した結果を報告いたしました。


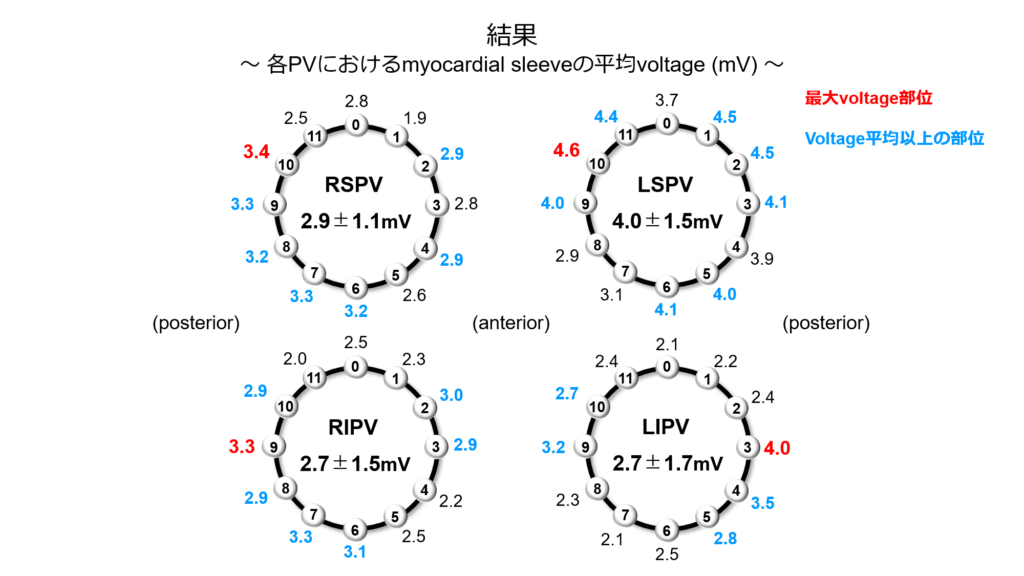
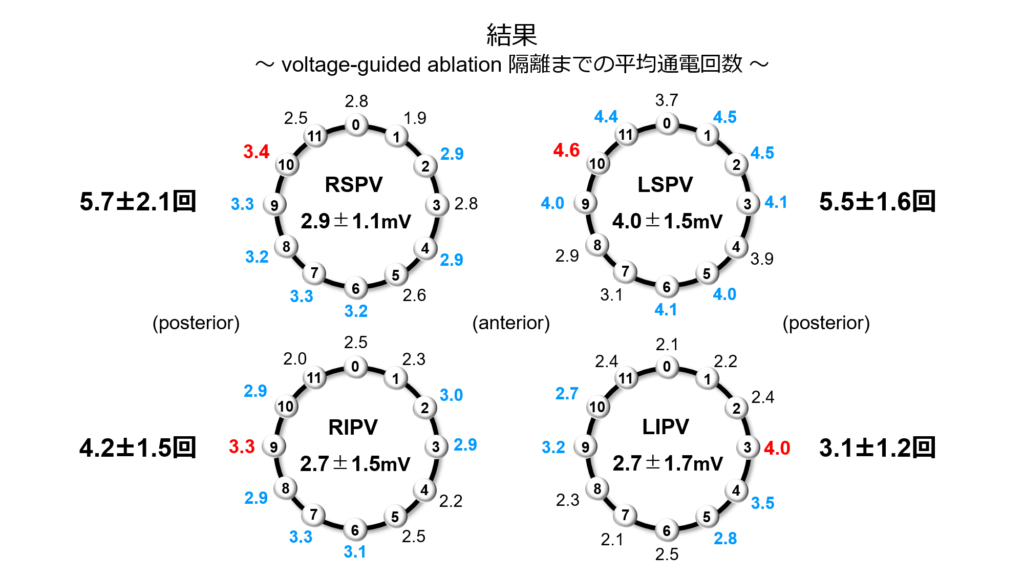
結果としてvoltageを指標とした個別隔離の平均回数は
右上肺静脈:5.7回 左上肺静脈:5.5回 右下肺静脈:4.2回 左下肺静脈:3.1回と
非常に良好な結果、つまり少ない回数で隔離が可能であるという結果が示されました。
発表後はたくさんのご質問も頂き、非常に有意義な新潟遠征となりました。
これからも皆様に、再発・合併症の少ない質の高いカテーテル治療をお届けできるよう日々努めていきたいと考えております。
なにかございまいたらお気軽にご相談を頂けましたら幸いです。
今年も宜しくお願い申し上げます!
院長の山嵜です。
大変遅くなりましたが、今年初のブログ更新となります。
昨年末より新型コロナウイルス感染症に加え、インフルエンザ感染症も増加傾向を認めており皆様も非常に不安な日々をお過ごしのことと思います。
一方感染症との共存に向けて社会活動が以前と同様の体制に戻っていくのも実感するところです。
いつどのような形で収束していくのかは想像が難しいところではございますが、地域の皆様に頼りにして頂けるクリニックであり続けたいとスタッフ一同考えておりますので、本年も何卒宜しくお願い申し上げます。
※昨年末はブログを更新する時間があまりございませんでしたので、これからしばらくは昨年書きそびれたことも投稿してまいりたいと思います。
横浜市青葉区における災害対策
院長の山嵜です。
本日は青葉区看護職連絡会・在宅医療連携拠点合同企画にお招きいただき、
「地域における防災研修 医療職・介護職が知っておくべき災害対策」
というテーマで講演をさせて頂きました。
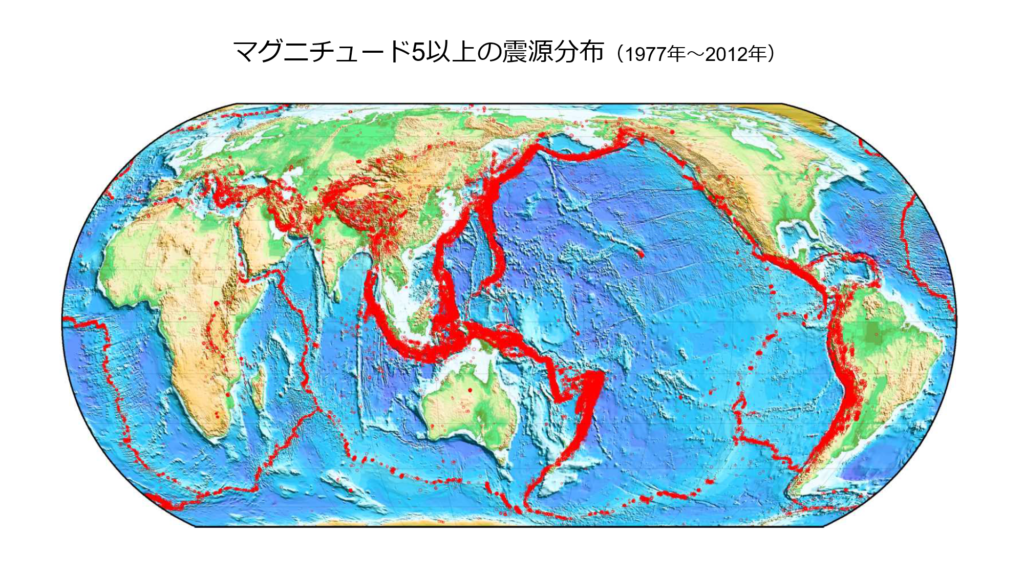
地震は世界中どこでも起こっているわけではなく、地震が多発する地域とそうでない地域があります。上の図は、世界地図の上に、1977年1月から2012年12月までに発生したマグニチュード5以上の地震を赤い丸印で示したものです。日本の面積は世界の面積の1%未満であるにもかかわらず、世界の地震の約1割が日本の周辺で起こっています。日本は世界的に見ても地震による危険度が非常に高く、全国のどこでも地震によって強い揺れに見舞われる可能性があります。
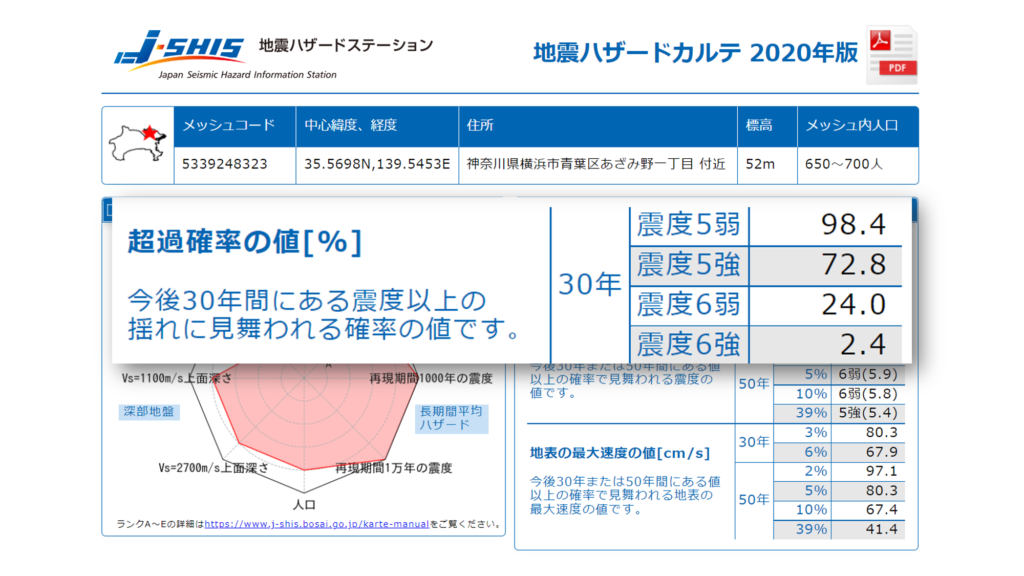
上の地震ハザードカルテによりますと青葉区医師会館の存在するあざみ野一丁目付近では、30年以内に震度5弱の揺れが発生する可能性が98.4%、5強が72.8%、6弱が24%、そして6強が2.4%と推定されています。
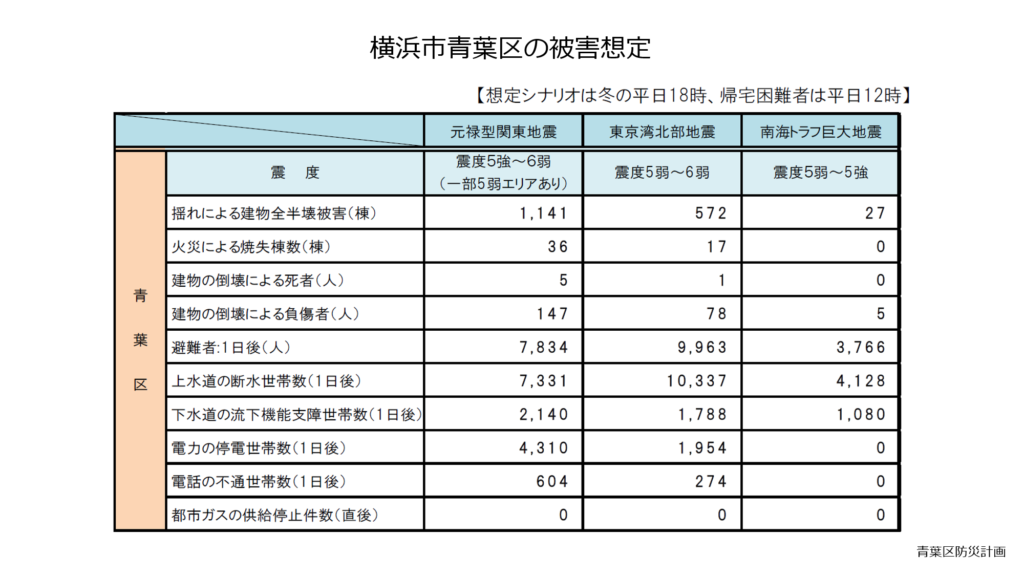
元禄型大地震が発生した際の横浜市青葉区の被害想定では、死者数は少ないものの発災一日後の推定避難者数は7,834人と多くの避難者が発生することが予測されています。
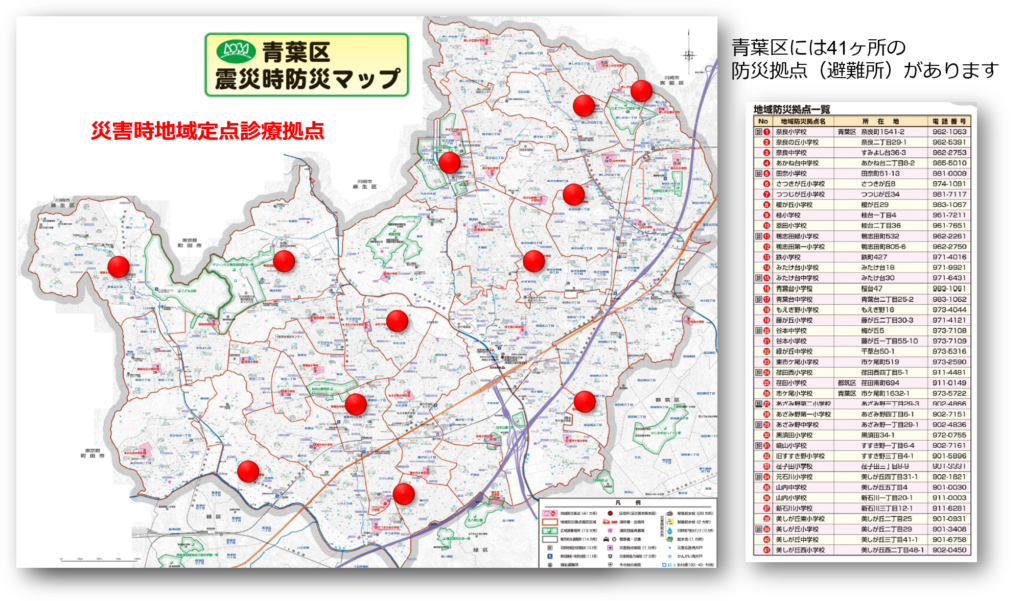
青葉区には41か所の避難所がありますが、うち12ヶ所には震度6弱以上の揺れが発生した際に定点診療拠点が開設されます。
定点診療拠点では下記のような活動が行われます。

青葉区医師会会員の先生方は震度6弱以上の揺れが発生したら、担当の定点診療拠点に参集することになっています。
自院での診療が可能な先生は黄色の診療旗を掲げて診療を行っていただき、自院での診療が困難な先生は定点診療拠点に残って、トリアージや診療に従事致します。
災害時に多数の診療拠点を開設するためには多くの医師の協力が必要です。一つの区内に12もの診療拠点を開設し活動することになっているのは横浜市18区の中でも青葉区だけです。
ご協力いただける先生方には感謝しかありません。
まだまだお話したことはたくさんありましたが、書ききれないのでまたの機会にその場を設けたいと思います。
本日は看護職・介護職の方をはじめとしてケアマネージャーさん、薬剤師の先生などなど50名を超す多職種の皆さんにご参加いただきました。
これだけの医療従事者の方が災害に対して興味を持っていただけたことは大変うれしく思います。
災害時には自助・共助・公助どれも欠かすことが出来ません。多くの方が一丸となって青葉区の災害対策を構築していけましたら幸いです。
本日もお疲れ様でございました。






